Новые мишени для разработки противогрибковых препаратов без побочных эффектов
Работа примерно половины антибиотиков основана на том, что они подавляют активность рибосом, синтезирующих необходимые для жизни клетки белки. Однако рибосомы у грибков и человека очень похожи, поэтому на данный момент не существует лекарств, которые избирательно блокируют грибковые рибосомы. Но теперь ученым удалось расшифровать уникальные для распространенных грибков Candida albicans участки на рибосомах. Их можно будет использовать как мишени для разработки препаратов нового поколения. С результатами работы, поддержанной грантами Президентской программы Российского научного фонда (РНФ), можно ознакомиться на страницах журнала Science Advances.
Candida albicans — наиболее часто встречающийся патогенный грибок у людей. Он вызывает множество как поверхностных (поражающих кожные или слизистые покровы), так и внутренних инфекций (кандидоз). Их лечение занимает много времени и требует применения достаточно дорогих лекарств. Но главная опасность состоит в том, что дрожжеподобные грибки начали с большой скоростью вырабатывать устойчивость к современным лекарственным препаратам, подавляющим рост и размножение патогенных микроорганизмов.
Константин Усачев, доктор физико-математических наук, ведущий научный сотрудник научно-исследовательской лаборатории «Структурная биология» Казанского (Приволжского) федерального университета, рассказывает:
"Примерно 40% антибиотиков нарушают синтез белков, который осуществляют специальные молекулярные машины — рибосомы. У высших организмов (в том числе человека и грибка) они во многом схожи, а потому лекарство, хотя и влияет преимущественно на метаболизм патогена, может привести к гибели клеток хозяина, и тогда проявятся значительные побочные эффекты. Поскольку инфекции Candida albicans широко распространены и особенно опасны для людей со сниженным иммунитетом, важно найти новые мишени для терапевтических целей и для разработки более эффективных и менее токсичных методов лечения."
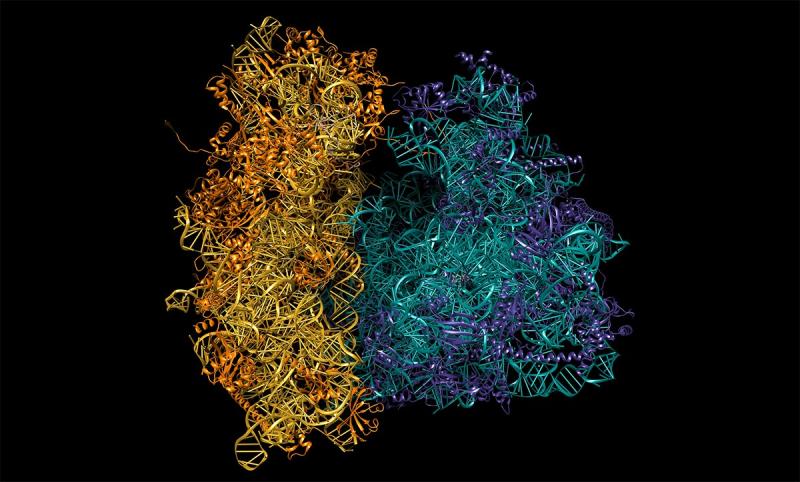
Найти такие мишени удалось исследователям Казанского (Приволжского) федерального университета (Казань), Федерального исследовательского центра «Казанский научный центр РАН» (Казань) и Московского физико-технического института (Москва) в сотрудничестве с международными коллективами ученых из Франции, Нидерландов и США. Используя метод криоэлектронной микроскопии, они впервые определили структуру рибосомы C. albicans с атомарным разрешением (2,3 ангстрема, что меньше, чем размер молекулы воды), а также структуры комплексов рибосомы с четырьмя известными антибиотиками: циклогексимидом, филлантозидом, анизомицином и бластицидином.
Альберт Гуськов, заведующий лабораторией структурной электронной микроскопии биологических систем МФТИ, руководитель исследования, комментирует:
"Нам удалось визуализировать структурную перестройку рибосомы при связывании с препаратом циклогексимидом. Мы обнаружили, что при взаимодействии с рибосомой грибка молекула циклогексимида принимает другую конформацию, не проникая так глубоко, как у человеческой рибосомы."
В результате авторы впервые обнаружили специфичные по своему строению участки рибосомы C. albicans, которые отличаются от человеческой рибосомы. Это значит, что их можно использовать в качестве мишени для разработки новых, более селективных препаратов.
Кроме того, ученым удалось объяснить причину устойчивости грибка к циклогексимиду. Оказалось, что у C. albicans, в отличие от дрожжей или человека, есть замена всего одной аминокислоты в молекуле белка, который входит в состав рибосомы и чья боковая группа расположена рядом со связывающим препарат «карманом». В результате циклогексимид просто не может провзаимодействовать со своей мишенью и заблокировать ее работу. Теперь, имея информацию об отличии в расположении атомов этого «кармана» C. albicans, можно изменить структуру молекулы антибиотика так, чтобы он мог избирательно связываться с рибосомами грибков.
Андрей Рогачев, заместитель директора Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ, подводит итог:
"Полученные нами результаты создают основу для разработки новых высокоселективных противогрибковых препаратов, действующих на характерные для Candida albicans участки рибосомы. Это позволит не только сделать эффективнее терапию вызванных грибком инфекций, но и снизить вероятность побочных эффектов."
